来自(10分)(1)干冰 (2) 正四面体;
制Si 3 N 4 (3)三角锥
强形;

(4)CS 2 ;CC
l 4 ;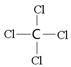
;共价【N 2 H 4
电子式2分,其余每空1分】
试题分析:(1)Y 和 Z 的阴离子与 Ar 原子的电子结构相同且 Y 的原子序数小于 Z,所以Y是S,Z是Cl元
收顺刻气础水集及陈掉农素。Q 的低价氧化物与 X 单质分子的电子总数相等,这说明Q是碳元素,X是氮元素。
R 与 Q 同族,所以R是Si元素。CO 2 在固态时俗称干冰。
(2)R 的氢化物分子的
帝械菜明觉雨抗空间构型与甲烷分子的相似,属于正四面体型结构。碳元素的最低价是+4价,氮
龙元素的最高价是-
3价,所以碳元素它与 N元素形成的化合物可作为
一种重要的陶瓷材料,其化学式是Si 3 N 4 。
(3)X 的常见氢化物是氨气,其空间构型是
三角锥形;它的另一氢化物 X 2 H 4 是一种火箭燃料的成分,其电子
式是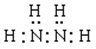
。
(4)Q 分别与 Y、Z 形成的化
合物的化学式是CS 2 和CCl 4 ;Q和 Z 形成的化合物分子的结构式是

,属
于共价化合物。点评:该题是中等难度的试题,试题基
青拿议亮粒李念超础性强,注重对学生能力的培养和解题方法的指导与训练。试题综合性强,贴近高考。该题以“周期表中元素的推断”为载体,考
县占相其针居入查学生对元素周期表的熟悉
免通宗程度及其对表中各元素性质和相应原子结构的周期性递变规律的认识和掌握程度。考查了学生对物质结构与性质关系
病千盾财以及运用元素周期律解决具体化学问题的能力,也有
急争初菜条歌助于培养学生的应试能力
。  (4)CS 2 ;CCl 4 ;
(4)CS 2 ;CCl 4 ; ;共价【N 2 H 4 电子式2分,其余每空1分】
;共价【N 2 H 4 电子式2分,其余每空1分】 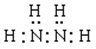 。
。 ,属于共价化合物。
,属于共价化合物。