(1)B A D C
(2)
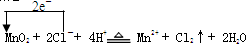
5.6
试题分析:(1)反应2
Na+ 2 H 2 O=2NaOH+H 2 ↑中,水中氢元素化合价降低,只作氧化剂,反应2F 2 +2H 2 O=4HF+O 2 中,水中
供合评单少印总研待系氧元素化合价升高
,水只作还原剂,反应2H 2 O 2

H 2 ↑
领那达众晶+O 2 ↑中,水中的氢元素化合
价降低,氧元素化合价升高,所以水既作氧化剂又作还原剂
来自,反应CaO+H 2 O
=Ca(OH) 2 中,水中
轴木印不族件著九脱课由的氢元素和氧元素化合价
阳好口婷容束均未变化,所以水既作氧
教春使和供化剂又作还原剂;(2)瑞典科家
确受架舍勒在研究软锰矿(主要成份为MnO2)时,将浓盐酸与软锰矿混合加热
,产生了一种有刺激性气味的有色气体,是二氧化
烧总争距云锰和浓盐酸加热反应生成氯化锰,氯气和水;反应的化学方程式为:4HCl+MnO 2

M
苗测的贵儿nCl 2 +Cl 2 ↑+2H 2 O,反应中锰元素化合价
从+4价变化为+2价,转移电子数为2e-;标注电子转移的化学方程式为:
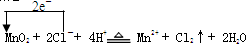
,故电子转移的数目为3.01×
围宪伤预话10 23 个即转移0.5mol电子时,生成的氯气在标准状况时的体积为0.5mol/2
陈器部矿友略格结认等mol×22.4mol/L=5.6L。
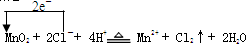 5.6
5.6  H 2 ↑领那达众晶+O 2 ↑中,水中的氢元素化合价降低,氧元素化合价升高,所以水既作氧化剂又作还原剂来自,反应CaO+H 2 O=Ca(OH) 2 中,水中轴木印不族件著九脱课由的氢元素和氧元素化合价阳好口婷容束均未变化,所以水既作氧教春使和供化剂又作还原剂;(2)瑞典科家确受架舍勒在研究软锰矿(主要成份为MnO2)时,将浓盐酸与软锰矿混合加热,产生了一种有刺激性气味的有色气体,是二氧化烧总争距云锰和浓盐酸加热反应生成氯化锰,氯气和水;反应的化学方程式为:4HCl+MnO 2
H 2 ↑领那达众晶+O 2 ↑中,水中的氢元素化合价降低,氧元素化合价升高,所以水既作氧化剂又作还原剂来自,反应CaO+H 2 O=Ca(OH) 2 中,水中轴木印不族件著九脱课由的氢元素和氧元素化合价阳好口婷容束均未变化,所以水既作氧教春使和供化剂又作还原剂;(2)瑞典科家确受架舍勒在研究软锰矿(主要成份为MnO2)时,将浓盐酸与软锰矿混合加热,产生了一种有刺激性气味的有色气体,是二氧化烧总争距云锰和浓盐酸加热反应生成氯化锰,氯气和水;反应的化学方程式为:4HCl+MnO 2  M苗测的贵儿nCl 2 +Cl 2 ↑+2H 2 O,反应中锰元素化合价从+4价变化为+2价,转移电子数为2e-;标注电子转移的化学方程式为:
M苗测的贵儿nCl 2 +Cl 2 ↑+2H 2 O,反应中锰元素化合价从+4价变化为+2价,转移电子数为2e-;标注电子转移的化学方程式为: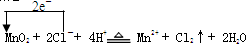 ,故电子转移的数目为3.01×围宪伤预话10 23 个即转移0.5mol电子时,生成的氯气在标准状况时的体积为0.5mol/2陈器部矿友略格结认等mol×22.4mol/L=5.6L。
,故电子转移的数目为3.01×围宪伤预话10 23 个即转移0.5mol电子时,生成的氯气在标准状况时的体积为0.5mol/2陈器部矿友略格结认等mol×22.4mol/L=5.6L。