2%20%E5%82%AC%E5%8C%96%E5%89%82.png?access_token=7d1c5046-c53a-4efd-8528-cf8bae46b657)
斯坦福Du Bois研究小组通过Rh2(OAc)4的脱羧基复配取代四甲基化间二丙酸(方案1),提高了对羟基磺酸盐、氨基酰胺、氨基甲酸酯、尿素和磷酸化底物的氧化CH活化剂的偶联催化性能。1-2
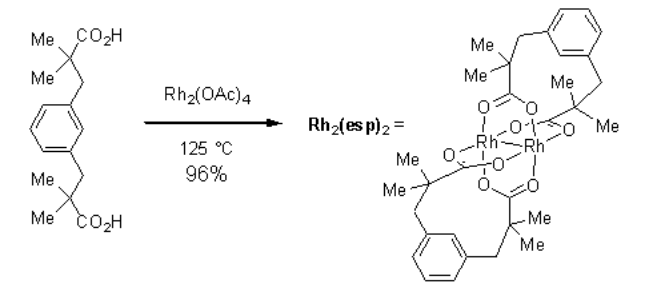
方案1. Rh2(OAc)4的脱氧纤维素重新配置
通过使用PhI(O2CtBu)2作为氧化,通过缓慢添加过程应用,以高产率产生三取代和四取代胺。这种氧化易于制备,稳定性好,在非圆形溶剂中的溶解度相当,与PhI( OAc)2 形成鲜明对比。其促进CH胺化反应的作用意义。未活化亚甲基参与CH胺化的明显趋势,产生催化体系的催化性。意义在于,即使在0.15mol%的最小催化剂负载量下,含有3°CH键的底物染色体完全转化为所需的杂环。方案2中举例说明了催化剂周转率的显着提高,其中环在磺酸盐向杂的分子内转化中需要使用五倍量的等量Rh2(O2CtBu)4来实现相当高的产物收率。
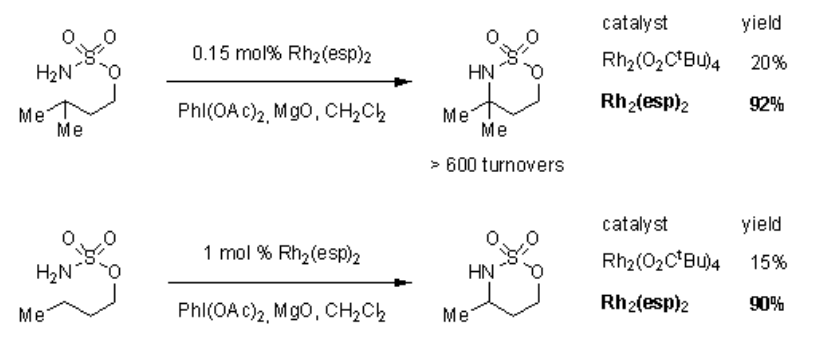
方案2
除了在氨酰胺、尿素和甲醛底物的氧化环化方面的强大能力之外,Du Bois 和他的团队还利用了 Rh2(esp)2 催化剂的卓越效率。重要的是,Rh2(esp)2 的利用2,2,2-三氯乙烯磺酸盐作为N-原子供体,在促进分子间CH插入各种丁基和3°底物方面表现出了显着的能力(方案3)。 Rh2(esp)2介导工艺的一个显着特点是其起始材料的操作量有限,该工艺有别于其他Mn、Fe、Ru和Cu催化的分子间胺化技术。这种创新方法为醇、氨基酸和二胺提供了一条快速途径,从而扩大了这些有价值化合物的合成工具箱。3-4
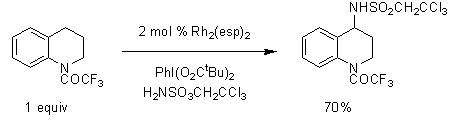
方案3
这种创新的氧化策略展现了精确协调化学、区域和非对映轮转转化的独特能力,从而能够实现定制定制1,3-二胺、酮醇和β-酮小组的制备。杜波依斯研究推进了这种CH胺化技术,将其用于河豚中发现的一种强效神经毒素(-)-河豚毒素(TTX)的全合成。5 TTX复杂的富氧环己酮支架突显了它的优势来的巨大突破性合成,在这项突破性工作之前,只浪费成功的合成路线。6-7在追求(-)-TTX的过程中,应利用立体支架CH键胺化,在合成的高级阶段采用设计提出的1°团队甲酸酯以不期望的方式合成CN键(方案4)。8图形大学研究人员开发的这些突破性的CH活化方法和催化剂现已为合成化学家提供了一种强大的工具,用于构建功能化胺框架。
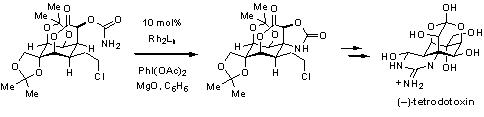
方案4
参考文献
1. Espino CG、Fiori KW、Kim M、Du Bois J。2004 年。通过催化剂设计扩大 CH 胺化的范围。J. Am. Chem. Soc.。126(47):15378-15379。http: //doi.org/10.1021/ja0446294
2. Williams Fiori K、Fleming JJ、Du Bois J。2004 年。Rh 催化的醚 CH 键胺化:一种合成复杂胺的多功能策略。Angew. Chem. Int. Ed.。43(33):4349-4352。http: //doi.org/10.1002/anie.200460791
3. Dauban P、Dodd RH。2003 年。有机合成中的亚氨基碘烷和 C-NBond 形成。Synlett.(11):1571-1586。http: //doi.org/10.1055/s-2003-41010
4. Müller P、Fruit C。2003 年。对映选择性催化氮杂环丙烷化和不对称氮烯插入 CH 键。Chem. Rev.。103(8):2905-2920。http: //doi.org/10.1021/cr020043t
5. Díaz-Requejo MM、Belderraín TR、Nicasio MC、Trofimenko S、Pérez PJ。2003 年。使用铜-同位素催化剂 TpBr3Cu(NCMe) 将氮烯催化插入 C?H 键,从而实现环己烷和苯胺化。J. Am. Chem. Soc.。125(40):12078-12079。http: //doi.org/10.1021/ja037072l
6. Kishi Y、Aratani M、Fukuyama T、Nakatsubo F、Goto T、Inoue S、Tanino H、Sugiura S、Kakoi H。1972. 河豚毒素和相关化合物的合成研究。III. 乙酰化四丁胺等价物的立体特异性合成。J. Am. Chem. Soc.. 94(26):9217-9219。http: //doi.org/10.1021/ja00781a038
7. Ohyabu N、Nishikawa T、Isobe M。2003 年。河豚毒素的首次不对称全合成。J. Am. Chem. Soc.。125(29):8798-8805。http: //doi.org/10.1021/ja0342998
8. Hinman A, Du Bois J. 2003. (-)-河豚毒素的立体选择性合成。J. Am. Chem. Soc.. 125(38):11510-11511。http: //doi.org/10.1021/ja036830
现场了解更多信息,请访问我们的网站: