| 服务名称 | 非靶向代谢组服务 |
| 提供商 | 上海鹿明生物科技有限公司 |
 |
 |
 |
 |
 |
 |
前言
农业增产及产品品质提升一直都是生物课题研究中重要的一部分,特别是稀有和低产物种。白灵菇是一种珍贵的珍稀食用菌,具有极高的营养和药用价值。本文为鹿明生物合作客户中国农业科学院农业资源与农业区划研究所胡清秀博士团队在Frontiers in Microbiology发表的 “白灵菇菌丝体生理成熟过程中的代谢轮廓谱分析及潜在菌丝体指示因子的探索”的文章。文章报道通过GC-MS非靶标代谢分析,发现N-氨基甲酰基L-天冬氨酸(CA-asp)可作为评估菌丝体成熟度的潜在指标,揭示了白灵菇菌丝体生理成熟期的代谢调控网络变化机制。

英文标题:Metabolic Profiling of Pleurotus tuoliensis During Mycelium Physiological Maturation and Exploration on a Potential Indicator of Mycelial Maturation
中文标题:白灵菇菌丝体生理成熟过程中的代谢轮廓谱分析及潜在菌丝体指示因子的探索
材料:白灵菇
影响因子:4.259
发表期刊:Frontiers in Microbiology
主要运用鹿明生物技术:GC-MS非靶标代谢组
研究背景
白灵菇是一种珍贵稀有的食用菌,具有极高的营养和药用价值。由于栽培技术尚不成熟,导致产量和质量波动较大。培育难点在于评估菌丝体的成熟度,目前缺乏可明确表征菌丝体生理成熟程度的量化指标。本研究的目的是通过GC-MS代谢组学的方法来研究白灵菇菌丝体生理成熟的潜在指标,进而改进白灵菇栽培方法,最大限度地提高产量和质量。
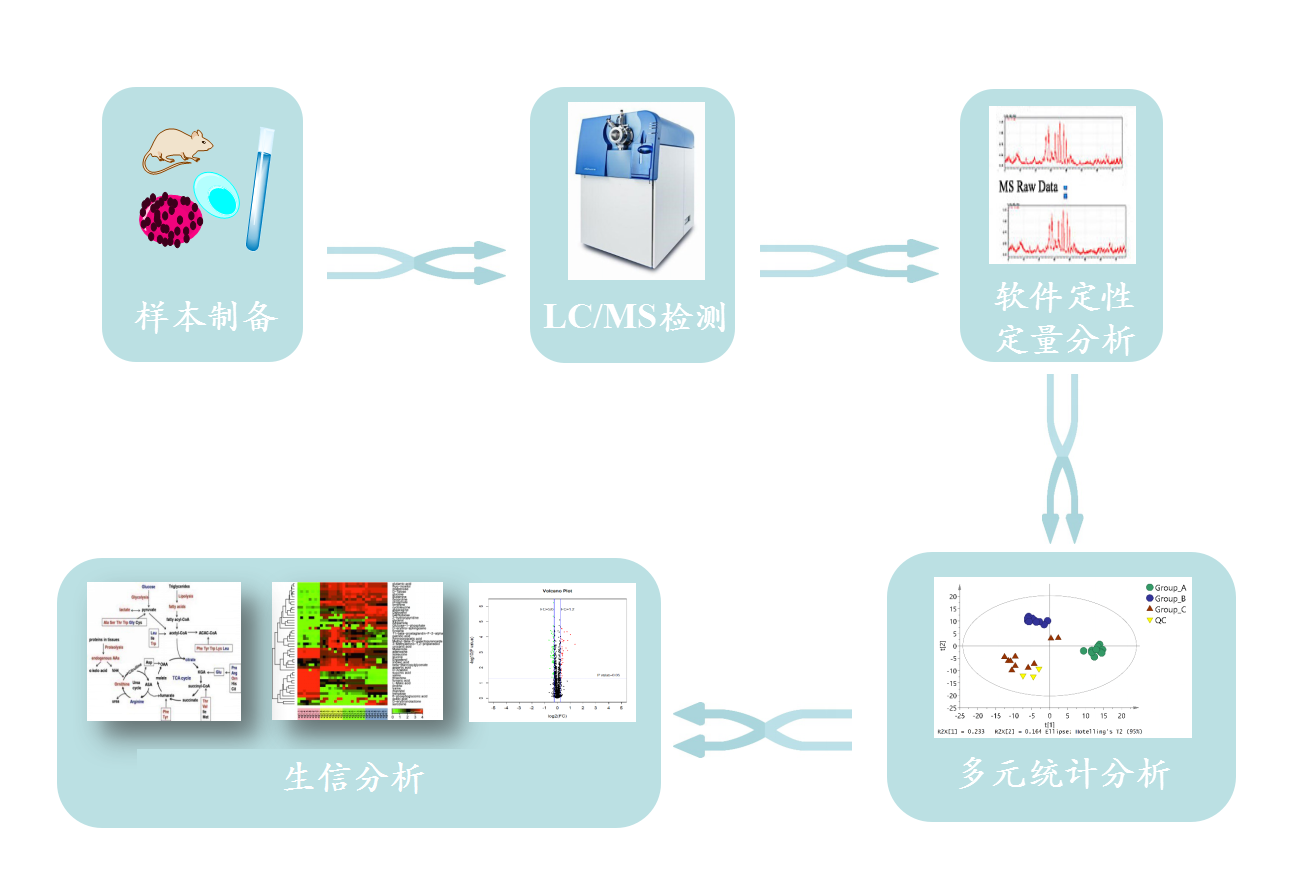
研究思路
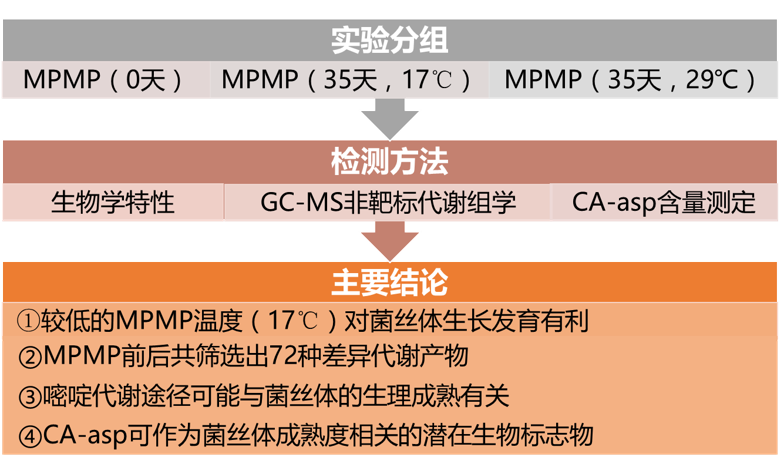
1.基于GC-MS的生理成熟菌丝体的代谢特征
为了调查MPMP过程中菌丝体的代谢变化,采用GC-MS代谢组学方法分析了第0天、第35天17℃和第35天29℃菌丝体的细胞外液样品(A、B和C样品)。三个样品共鉴定出236种代谢物。采用多元统计分析的方法,处理数据并得到差异代谢物。
2.多元统计分析
首先采用无监督的PCA分析来评估所有样品之间的总体分布以及整个分析过程的稳定性。如图2所示,PCA图的四个主要成分解释了59.1%的总方差信息。所有的QC(质量控制)样品均聚在一起,表明具有良好的分析稳定性和实验可重复性。在PCA模型中,三组样品在第一组分之间很好地分离,表明三组之间具有明显的代谢多样性。其中菌丝体A样品浓度更高,与菌丝体B和菌丝体C样品略有不同。这些结果与先前推测一致,即MPMP前后菌丝体细胞外液中的代谢谱差异很大。
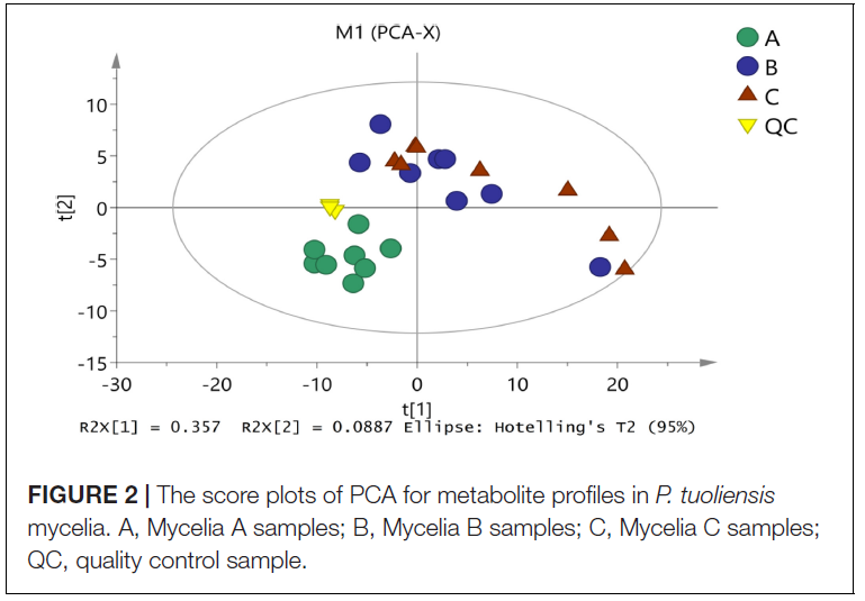
图2 | PCA得分图显示了白灵菇菌丝体中的代谢轮廓谱
A,菌丝体A;B,菌丝体B;C,菌丝体C;QC,质量控制样品
有监督PLS-DA模型显示,菌丝体A,B和C样品之间存在明显代谢差异(图3A,C,E)。PLS-DA模型的拟合度和预测能力均比较可信(表3),并未过拟合(图3B,D,F)。
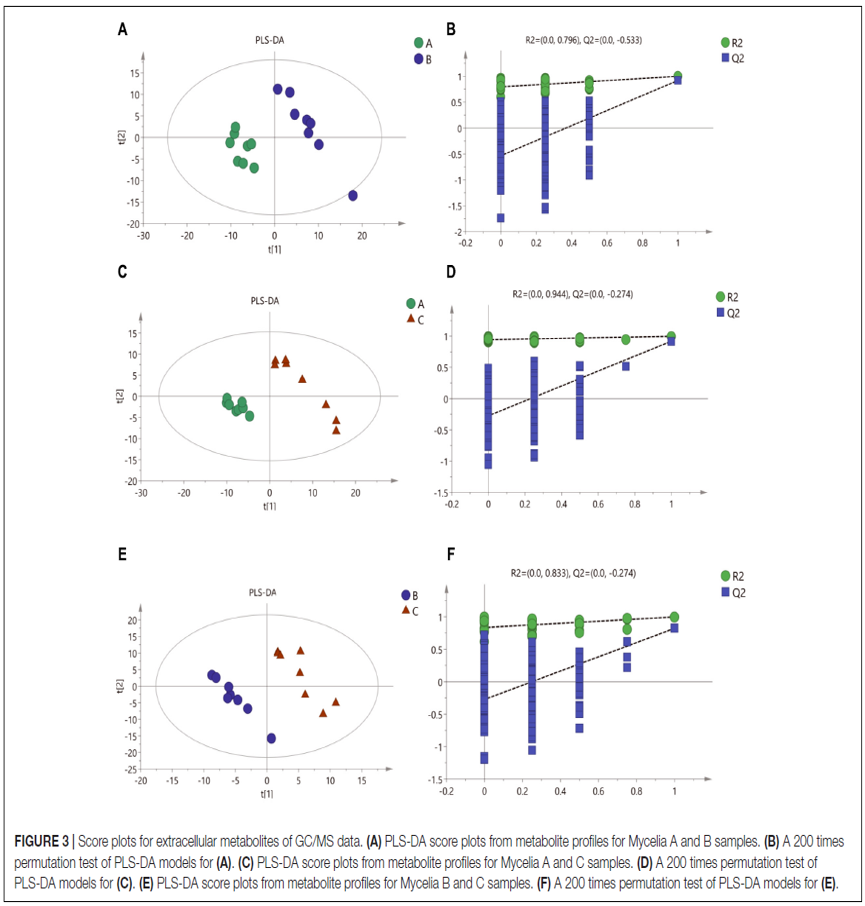
图3 | 基于GC / MS数据的细胞外代谢物得分图
(A)来自菌丝体A和B样品代谢轮廓谱的PLS-DA得分图;
(B)对(A)的PLS-DA模型进行200次排列检验;
(C)来自菌丝体A和C样品代谢轮廓谱的PLS-DA评分图;
(D)对(C)的PLS-DA模型进行200次排列检验;
(E)来自菌丝体B和C样品的代谢轮廓谱的PLS-DA得分图;
(F)对(E)的PLS-DA模型进行200次排列测试。
4.差异代谢物
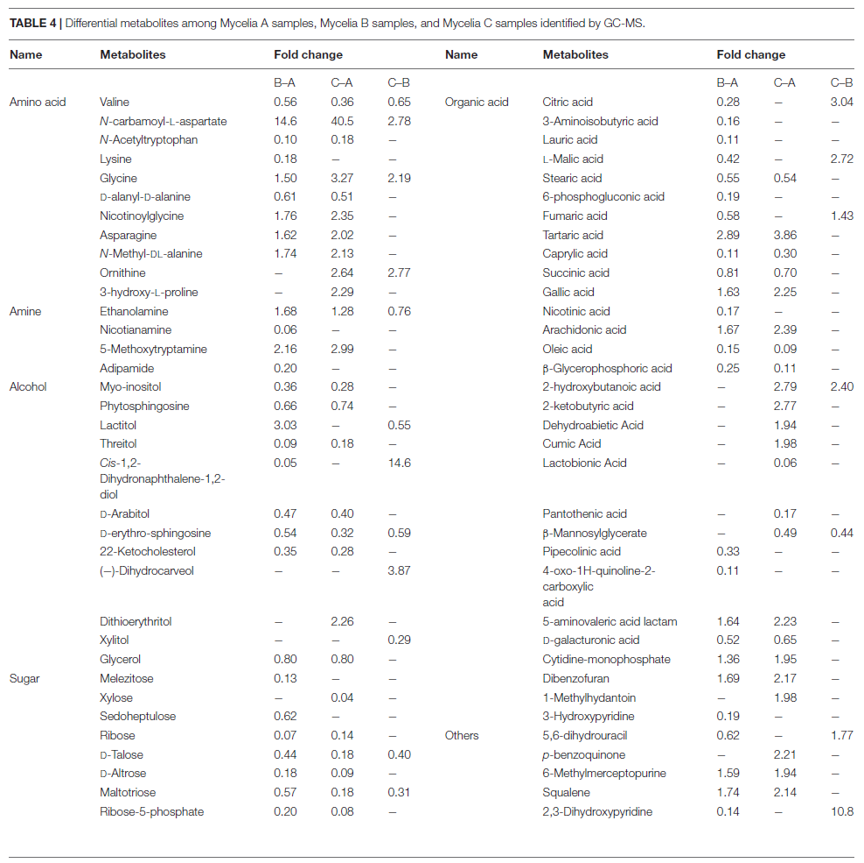
使用VIP值对样品之间的差异代谢物进行筛选,并通过非参数Mann-Whitney U检验进行确认。在三组样品中共鉴定出117种VIP值大于1.0且p <0.05的差异代谢物,包括41种有机酸、21种氨基酸、14种醇、11种糖、8种胺、5种酮、1种酯和16种其他代谢物。在MPMP第0天收集的菌丝体中很少检测到某些代谢物(A样品),而在第35天收集的菌丝体(B和C样品)中却显示出大量增加的代谢物,例如CA-asp、柠康酸、二氢香芹酚、褪黑激素和奎丁-4-羧酸。根据VIP值大于1.0和p <0.01的标准鉴定出72种差异代谢物(表4)。
表4 通过GC-MS鉴定的菌丝体A,B和C样品之间的差异代谢物
在菌丝体A,B和C样品的热图中观察到了差异代谢物明显的动态变化(图4A)。图4A的上部显示了与菌丝体A样品相比,菌丝体B和菌丝体C样品中丰度明显降低的代谢物,而图4A的下部显示了与菌丝体A样品,例如CA-asp、甘氨酸、乳糖醇、酒石酸、内酰胺、角鲨烯、6-甲基巯基嘌呤、5-甲氧基色胺、天冬酰胺、没食子酸和烟酰甘氨酸。图4B显示了与菌丝体B样品相比菌丝体C样品中的差异代谢产物。与菌丝体C样品相比,菌丝体B样品中丰度显著增加的代谢物包括缬氨酸、6-磷酸葡萄糖酸、D-塔洛糖、β-甘露糖基甘油酸酯、木糖醇、半乳糖醇、乳糖醇和麦芽三糖。而(-)-二氢香芹酚、2-羟基、柠檬酸、5,6-二氢尿嘧啶、L-苹果酸、马来酸、甘氨酸和鸟氨酸的丰度显著降低。
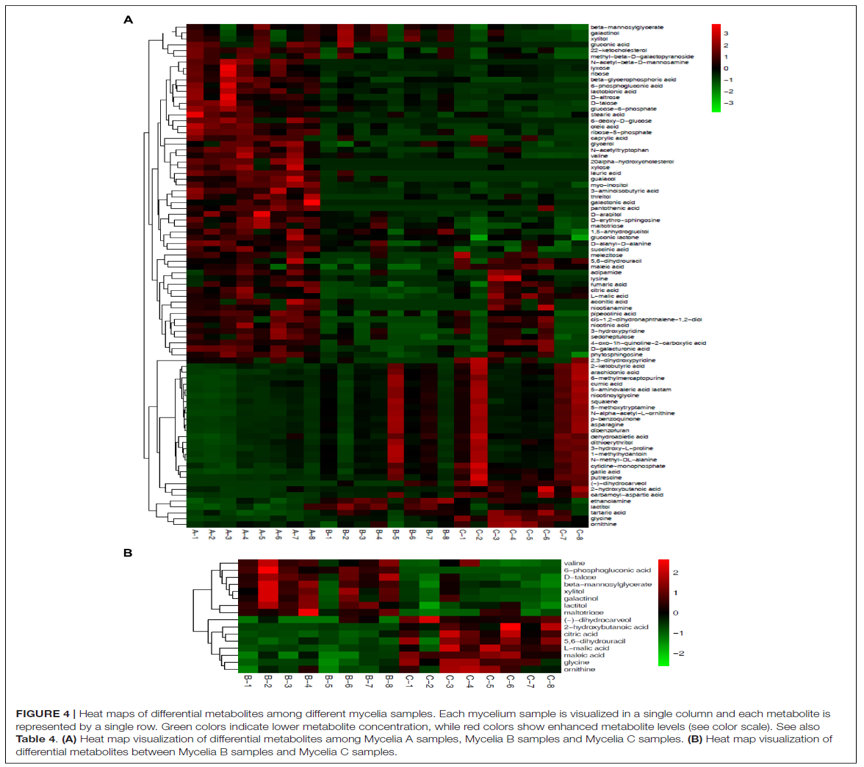
图4 | 不同菌丝体样品之间差异代谢物的热图
(A)菌丝体A,B和C样品之间差异代谢物的热图;
(B)菌丝体B样品和菌丝体C样品之间差异代谢物的热图;
列代表每个菌丝体样品,行代表每个代谢物;绿色表示较低的代谢物浓度,而红色表示较高的代谢物水平,参见表4。
图5显示了菌丝体B样品和菌丝体A样品之间(A),菌丝体C样品和菌丝体A样品之间(B)以及菌丝体C样品和B样品之间(C)的代谢物的相关性分析。较大的值表明两种代谢物之间的相关性更大。
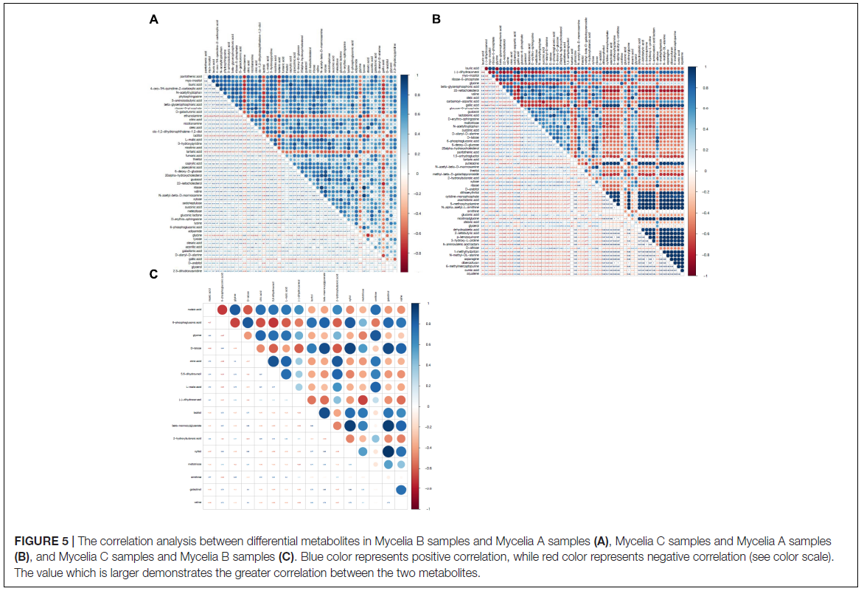
图5 | 差异代谢产物之间的相关性分析图
(A)菌丝体A和B样品,(B)菌丝体C和A样品,(C)菌丝体C和B样品。
蓝色代表正相关,而红色代表负相关,值越大表明两种代谢物之间的相关性更大。
5.代谢通路分析
为了深入了解三组样品之间代谢网络的差异,将确定的72种差异代谢物进行代谢途径富集分析。图6显示了菌丝体B和菌丝体A样品,菌丝体C和菌丝体A样品以及菌丝体C和菌丝体B样品之间的富集途径,包括五个主要的代谢途径——糖酵解、有机酸代谢、氨基酸代谢、三羧酸循环(TCA)和糖代谢。以及一些次级代谢途径——烟酸和烟酰胺代谢、氧化磷酸化。
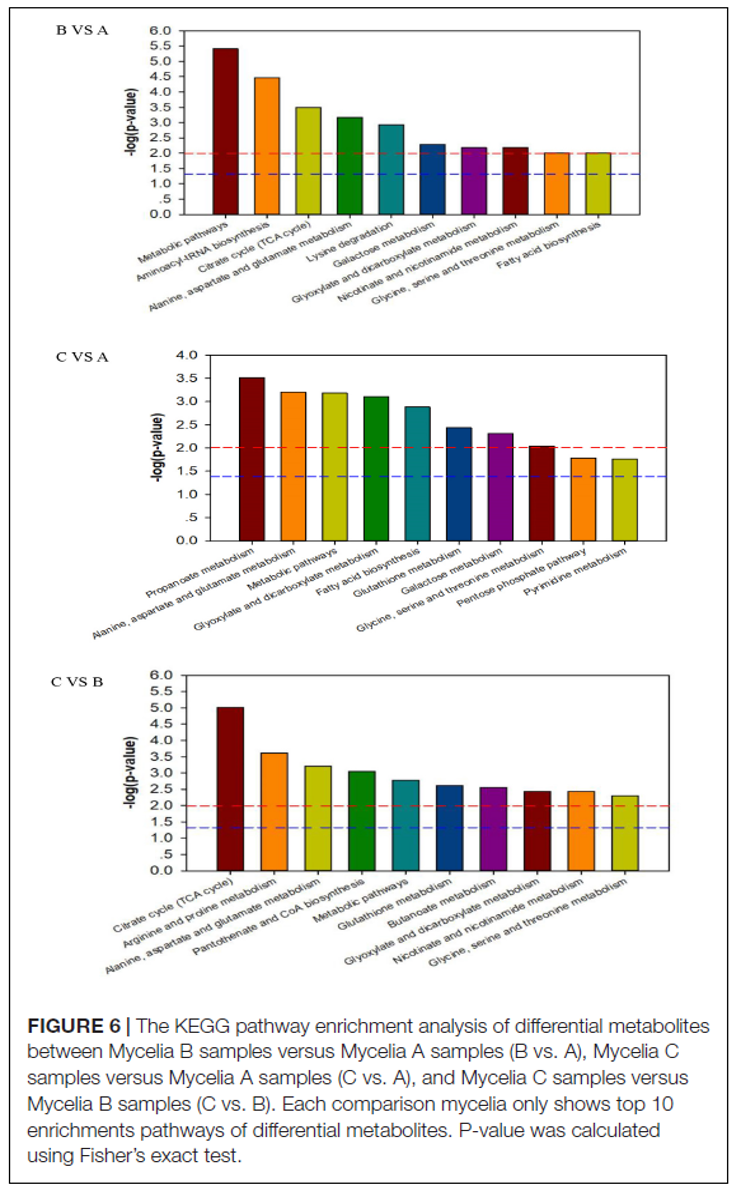
图6 | 差异代谢物的KEGG途径富集分析图
B vs. A菌丝体B与A样品,C vs. A菌丝体C与A样品,C vs. B菌丝体C与B样品。每组比较的菌丝体仅显示前10个差异代谢物的富集途径。P值使用Fisher精确检验计算得出的
图7显示了每种代谢途径中涉及的一些显著改变的途径和差异代谢物。
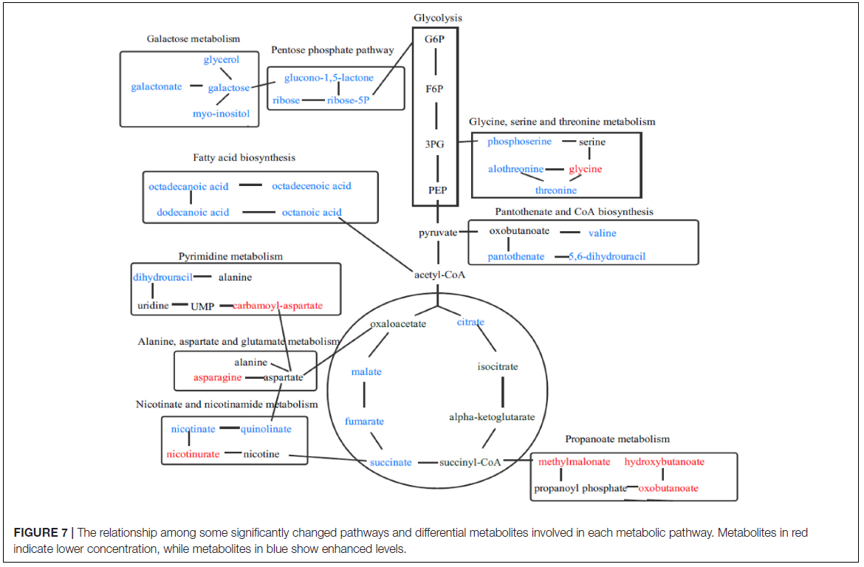
图7 | 某些显著改变的途径与每条代谢物途径所涉及的差异代谢物之间的关系
红色表示代谢物浓度较低,而蓝色表示代谢物浓度升高
图8仅显示了在MPMP第35天被显著激活的整个嘧啶代谢途径。
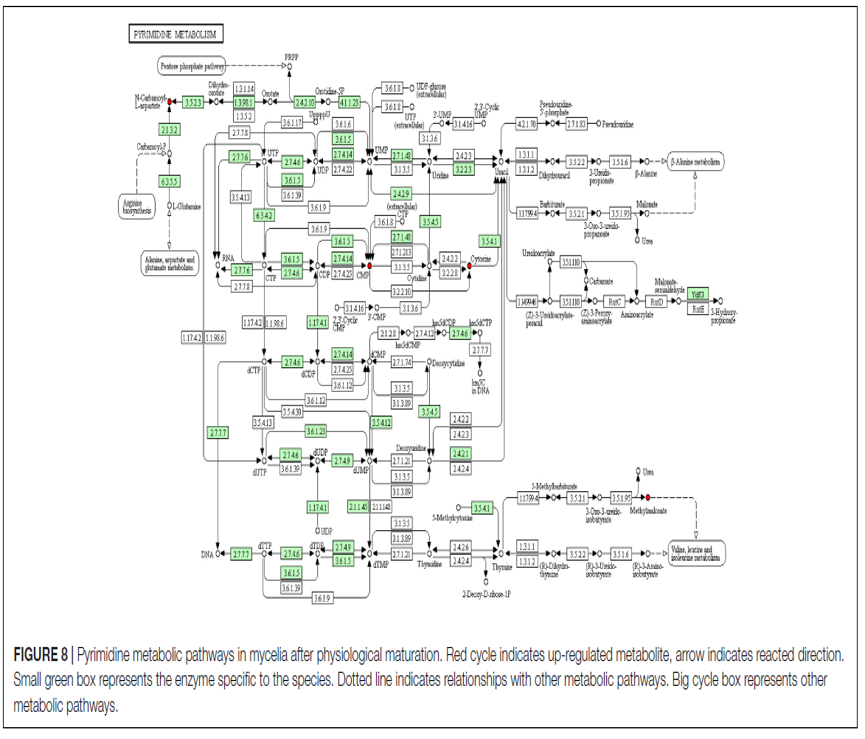
图8 | 生理成熟后菌丝体的嘧啶代谢途径
红色循环表示代谢物上调,箭头表示反应方向,小绿框代表该物种特有的酶,虚线表示与其他代谢途径的关系,大循环框代表其他代谢途径
实验结论
白灵菇的生物特征结果表明较低的MPMP温度(17℃)对其生长发育有利。采用基于GC-MS的非靶标代谢方法来比较在MPMP第0天、第35天(17℃和29℃)菌丝体中代谢产物的丰度,鉴定出236种差异代谢产物,根据VIP大于1和p <0.01的标准选择出72种差异代谢产物(上调37.8%,下调62.2%)。这些代谢物主要参与糖酵解、有机酸代谢、氨基酸代谢、TCA循环、糖代谢、烟酸酯和烟酰胺代谢以及氧化磷酸化。嘧啶代谢途径可能与菌丝体的生理成熟有关,参与该途径的代谢产物CA-asp的含量在MPMP第35天显著增强,是菌丝体成熟的潜在指标。作者证明了CA-asp在不同MPMP阶段收集菌丝体中的含量呈规律性变化,这表明CA-asp可用作菌丝体成熟指标的可行性,但该指标是否可用于商业生产需经大规模验证。
小鹿智囊 非靶向代谢组学
1、代谢组研究相对于基因组和蛋白质组研究而言有什么不同之处?主要特点包括三方面:一、基因和蛋白表达的有效的微小变化会在代谢物上得到放大,从而使检测更容易;二、代谢组学的技术不需建立全基因组测序及大量表达序列数据库;三、因为代谢产物在各个生物体系中都是类似的,所以代谢组学研究中采用的技术更通用。
2、代谢组的样品重复性有什么要求?
代谢组学基于多元统计分析方法进行的,在样品准备上相对于转录组和蛋白质组而言需要更多的重复数据。一般建议植物样品:最少6次,建议8次生物学重复;
模式动物及微生物样品:最少8次,建议10次生物学重复;
临床样品:30次生物学重复以上,如组织样品不好取样,可控制在20次重复以上。
3、靶向代谢检测平台的选择?
GC-MS和LC-MS两种平台各有优势,主要是由目标化合物的理化性质决定,GC-MS适合易挥发性、分子量不太大的化合物,而且,离子源为EI,碎片信息多,有成熟的图谱库,便于化合物检索,对于非挥发性成分则需要衍生化;而LC-MS离子源为APCI或者ESI源,适合做中等或强极性的化合物,分子量范围广,灵敏度高,前处理简单,但是LC-MS的价格要贵点,因此可以根据实际情况选择合适的检测平台。
4、关于代谢组数据库问题,老师经常问起数据库是商业库还是自己建的库,类型?
GC-MS数据库:Nist、feihn;
LC-MS数据库:HMDB、Metlin、自建库(大连化物所-许国旺组)。